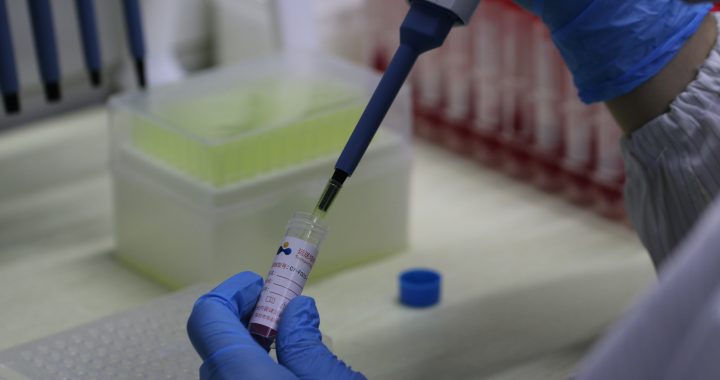
新冠病毒的核酸检测法
新型冠状病毒的检测方法主要包含核酸检测、抗体检测、抗原检测几种方法。由于抗原检测检出率较低,目前新冠检测主要集中在抗体和核酸检测。核酸检测目前是新冠病毒检测的“金标准”,具有早期诊断、灵敏度高和特异性高等特点;但抗体检测操作便捷、检测迅速,可作为核酸诊断的补充手段,但由于抗体检测“假阳性”和“假阴性”的局限性,不适合用于复工复产复学等普通人群筛查,也不适用于在低流地区的流行病学调查。
检测原理:
所有生物除朊病毒外都含有核酸,核酸包括脱氧核糖核酸(DNA)和核糖核酸(RNA)。新型冠状病毒(2019-nCoV)属于Beta冠状病毒属,该病毒是蛋白包裹的单链正链RNA病毒,寄生和感染高等动物(包括人)。病毒中特异性RNA序列是区分该病毒与其他病原体的标志物,新型冠状病毒出现后,我国科学家已经成功发现了新型冠状病毒中的特异性核酸序列。如疑似患者样本中能检测到新型冠状病毒的特异性核酸序列,则认为该患者可能被新型冠状病毒特异性核酸序列的方法是荧光定量PCR(聚合酶链式反应)。由于新型冠状病毒是RNA病毒,试剂盒检测基本都采用反转录加实时聚合酶链式反应法(RT-PCR),扩增病原体的核酸(RNA),同时通过荧光探针实时检测扩增产物。在PCR反应体系中,包含一对特异性引物以及一个Taqman探针,该探针为一段特异性寡核苷酸序列,两端分别标记了报告荧光基团和淬灭荧光基团。探针完整时,报告基团发射的荧光信号被淬灭基团吸收;如反应体系存在靶序列,PCR反应时探针与模板结合,DNA聚合酶沿模板利用酶的外切酶活性将探针酶切降解,报告基团与淬灭基团分离,发出荧光。每扩增一条DNA;链,就有一个荧光分子产生。荧光定量PCR仪能够监测出荧光到达预先设定阈值的循环数(Ct值)与病毒核酸浓度有关,病毒核酸浓度越高,Ct值越小。不同生产企业的产品会依据自身产品的性能确定本产品的阳性判断值。
由于每个RT-PCR反应需要2个小时左右才出结果,因此,试剂盒在开发时一般都针对病毒序列中高度保守的2~3各序列比如编码replicase(复制酶)或者necleocapsid(核蛋白衣,核鞘)的核酸序列设计引物,但是各个方法用的序列都不完全相同。一些方法使用multiplex,也就是把多个目标序列在同一反应管中扩增;另一些采用分步,先用一个目标序列筛查,阳性后再用另一个序列确认,这样可以有效缩短整个流程时间,加快检测速度。另外RNA病毒变异很快,用多个保守目标序列可以防止病毒变异造成的假阴性。
目前批准产品均基于新型冠状病毒基因组中开放读码框1a/b(open reading frame 1ab,ORF1ab)、包膜蛋白(Envelope protein,E)和核衣壳蛋白(nucleocapsid protein,N)进行选择。不同产品的检测原理基本一致,但是其引物、探针设计存在不同,有单靶区段(ORF1ab)、双靶区段(ORF1ab、N蛋白)、三靶区段(ORF1ab、N蛋白和E蛋白)的检测和判读差别。一般检测位于病毒ORF1ab和N基因上的两个靶标,同一份标本需满足双靶标阳性或重复检测为单靶标阳性或两种标本同时满足单靶标才能确认SARS-CoV-2病毒核酸阳性。
检测流程:
检测程序需要经过五个步骤,取样、留样、保存、核酸提取、上机检测。首先根据试剂盒说明书进行样本采集,样本类型包括咽拭子、鼻拭子、痰液、支气管灌洗液、肺泡灌洗液等。由于RNA易降解,因此,采集样本时使用无RNA酶的拭子和无RNA酶的储存管。获得患者样本后,需尽快进行检测,如无法立即检测需要进行低温封装,并送到专门的检测机构进行检测。检测机构收到样本后,对样本进行核酸提取,核酸提取试剂应使用批准产品说明书中指定的核酸提取试剂盒。最后是荧光PCR核酸检测,也就是上机器检测,将提取物进行荧光PCR扩增反应,需要70—80分钟。